آیا در آینده نزدیک خواهیم توانست از ارگانوئید ها بافت کلیه بسازیم و آن را جانشین کلیه های دچار نارسایی انسان کنیم؟
به گزارش صندلی و تلفن، در پزشکی احیا کننده، اگر بتوانیم سلول های بنیادی پرتوان انسانی (hPSCs) را رشد بدهیم و به سلول های مورد احتیاج خودمان تمایز بدهیم، انقلابی در درمان بیماری ها، از جمله بیماری های کلیوی ایجاد می گردد.
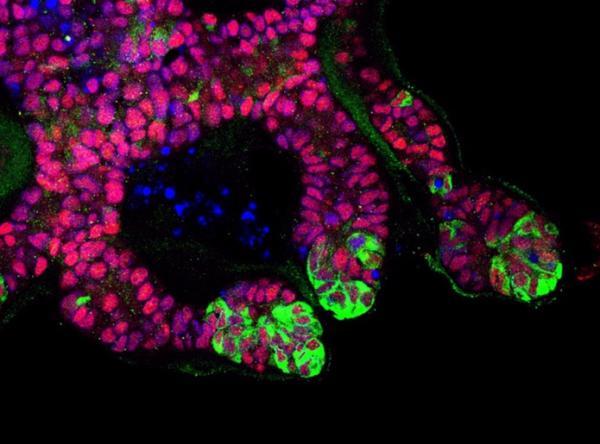
کلیه به طور طبیعی در انسان در نتیجه دو بلوک سازنده - مزانشیم متانفریک و جوانه حالب (UB) تشکیل می گردد. دانشمندان قبلاً کشف نموده بودند که چگونه اولین بلوک ساختمانی (مزانشیم متانفریک) را از از سلول های بنیادی بسازند.
اکنون، محققان روش بسیار کارآمدی را برای فراوری دومین بلوک ساختمانی (UB) یعنی سیستم جمع آوری کلیه، توسعه داده اند. به زبان فنی آنها می تانند hPSC ها را به ارگانوئید های UB و سلول های مجرای جمع نماینده عملکردی توسعه دهند.
علاوه بر این، آن ها ویژگی های تعامل بین سلول های این دو بلوک ساختمانی را نشان داده اند.
این تحقیق می تواند به محققان یاری کند تا درمان های تازهی را برای درمان بیماری های کلیوی که بر سیستم جمع آوری اثر می گذارند آزمایش نمایند. این موارد شامل بسیاری از ناهنجاری های مادرزادی کلیه و مجاری ادراری از جمله بیماری کلیه پلی کیستیک است.
این تحقیق در Nature Biotechnology در مقاله منتشر شده،
بیماری کلیوی از هر 9 بزرگسال یک نفر را در سراسر دنیا تحت تأثیر قرار می دهد و بروز نارسایی کلیه در سراسر دنیا به طور پیوسته در حال افزایش است.
محققان می گویند که برای اولین بار سلول های کلیه انسان را ایجاد نموده اند که می توان از آن ها برای پیشرفت دارو های تازه استفاده کرد، به آنالیز اختلالات ارثی و اکتسابی یاری کرد و درک پزشکان را از چگونگی رشد کلیه و کنترل تعادل متابولیک در بدن بهبود بخشید.
آن ها چطور این کار را کردند؟
نویسندگان نوشتند که hPSC ها ابتدا با کارایی 90 درصدی به سلول های پیش ساز پرونفریک القا می شوند و سپس در محفظه هایی مملو از مولکول های مشابه مجرای نفریک جمع می شوند. در یک ماتریکس سه بعدی، کره ها ارگانوئید های جوانه حالب را تشکیل می دهند.
آن ها نوشتند که در مراحل بعدی، ارگانوئید های جوانه حالب به ارگانوئید های مجرای جمع نماینده تمایز می یابند که حاوی بیش از 95 درصد انواع سلول های مجرای جمع نماینده هستند. این امر با توالی یابی RNA تک سلولی حاصل شد. این اپیتلیوم عملکرد های الکتروفیزیولوژیک کلیه را نشان داد.
در نهایت، با توانایی فراوری هر دو جزء مسئول ساخت بافت عملکردی کلیه، این کار گام بزرگی به جلو در کوشش برای جایگزینی عملکرد کلیه در بیماران مبتلا به نارسایی کلیه یا شاید در آینده فراوری کلیه آزمایشگاهی است.
منبع: یک پزشک